9L/lacZ-Zellen



















Allgemeine Informationen
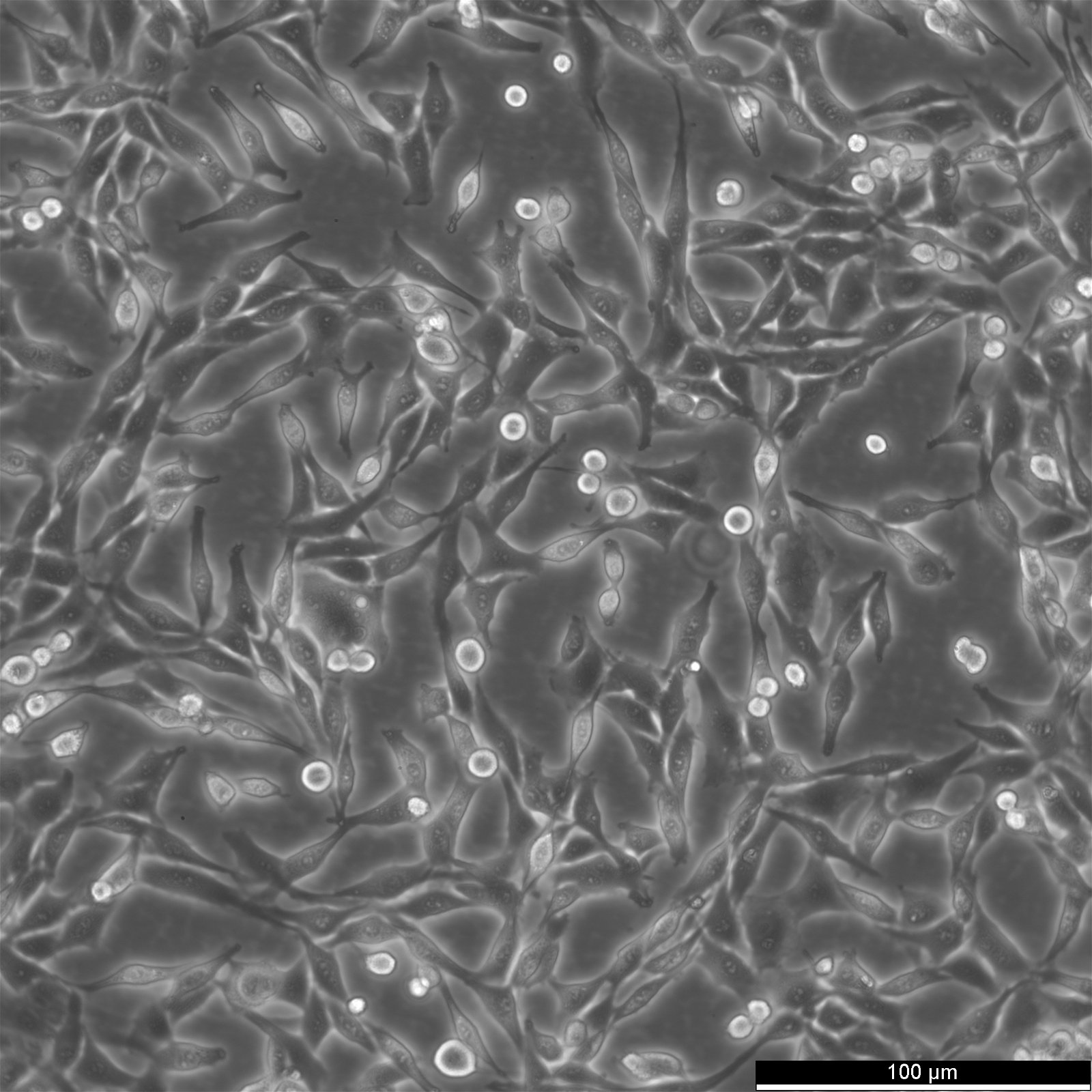
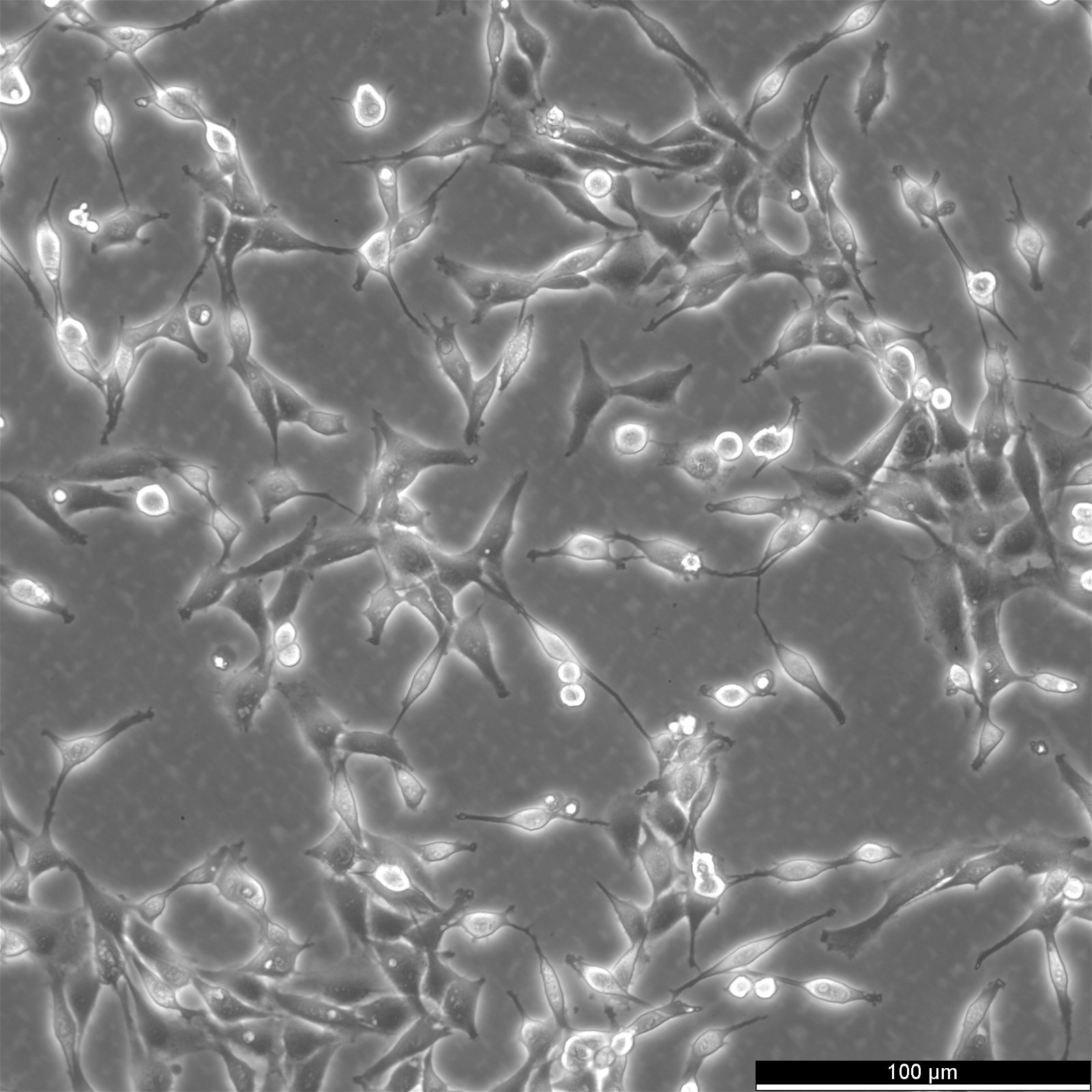
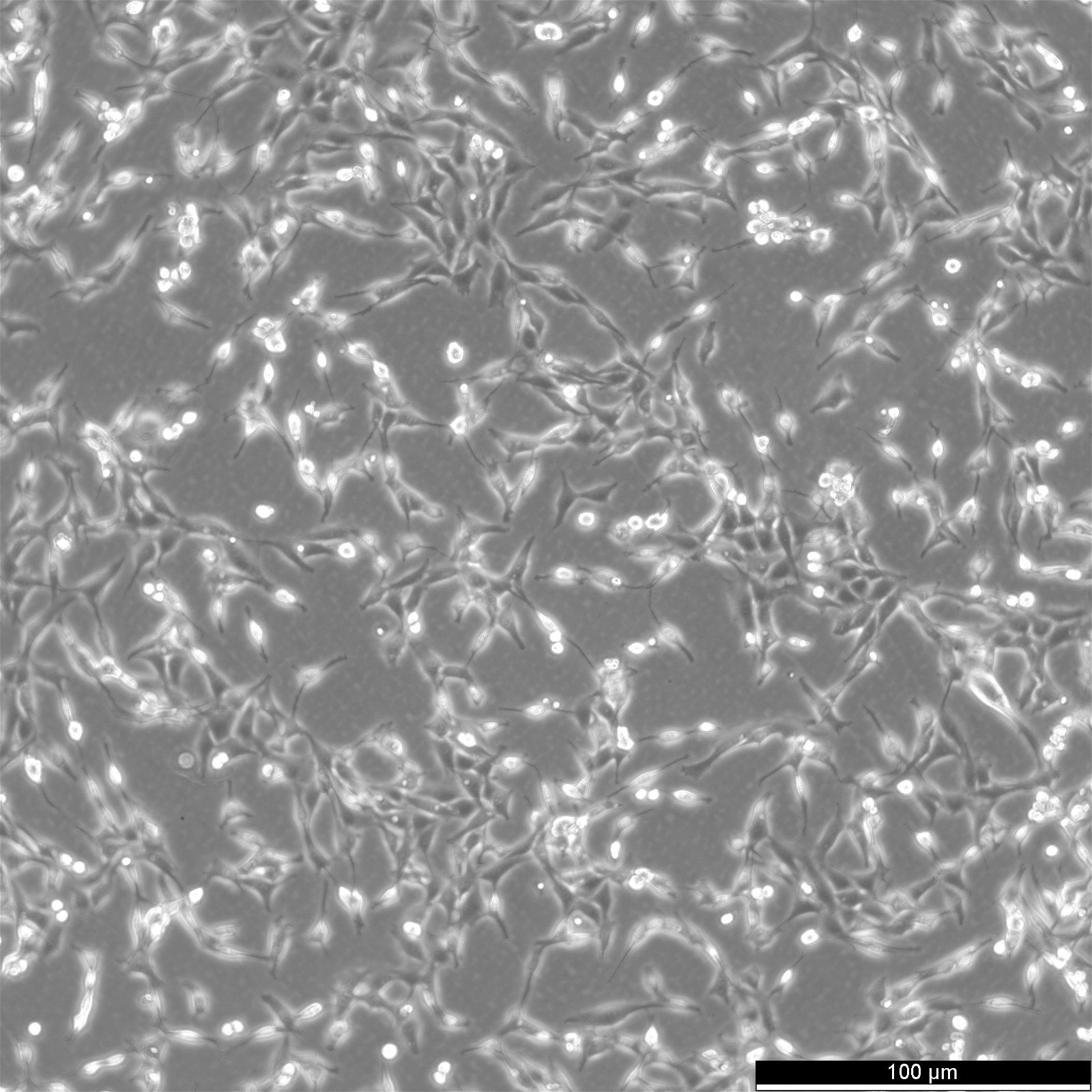
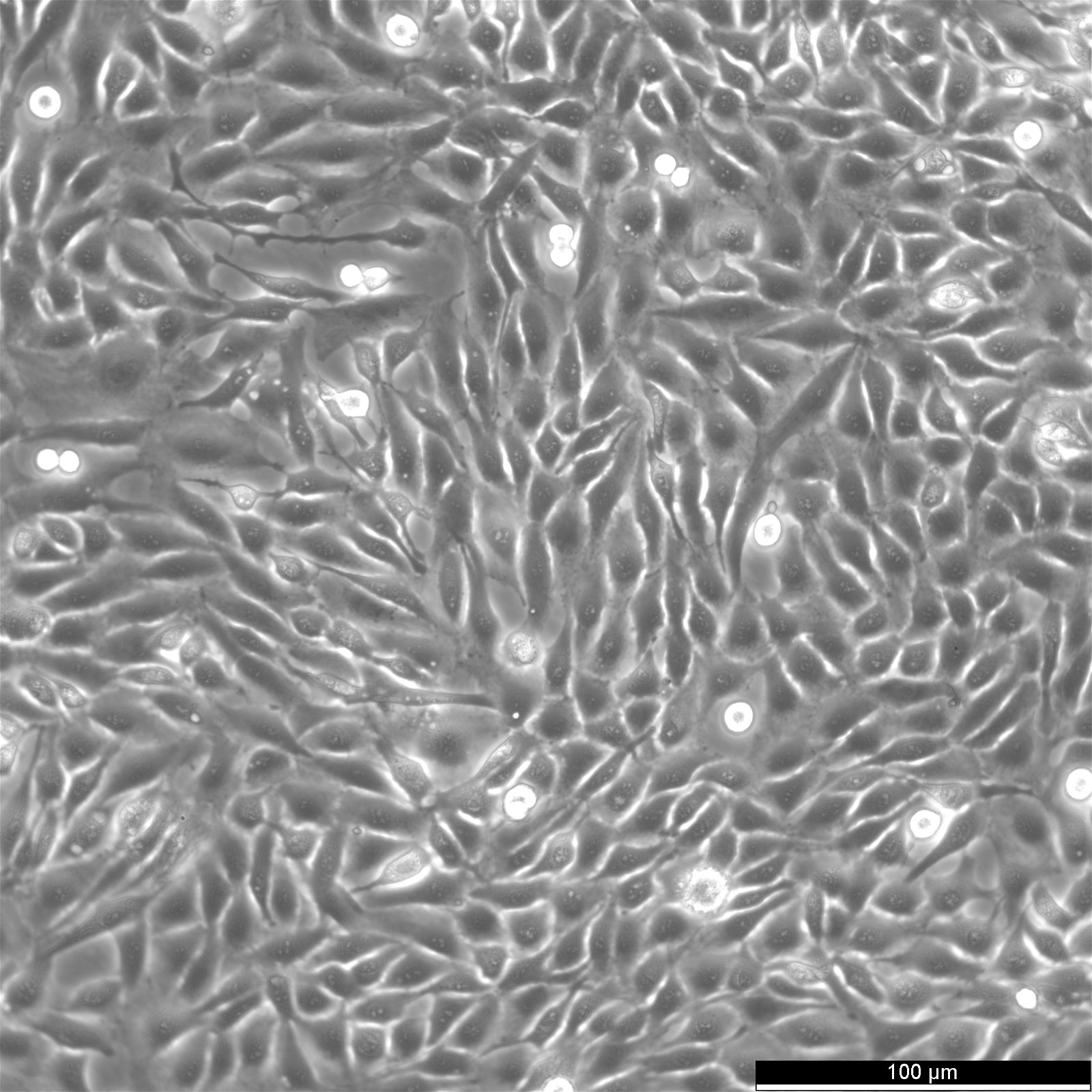
| Beschreibung | Die 9L/lacZ-Zelllinie, die aus Gliazellen von Rattus norvegicus (Ratten) stammt, weist eine Fibroblastenmorphologie auf und ist aus der 9L-Zelllinie hervorgegangen, einer durch Nitrosoharnstoff induzierten Gliosarkom-Zelllinie der Ratte. Die 1989 entwickelte 9L/lacZ-Zelllinie wurde durch die Infektion von 9L-Zellen mit dem retroviralen BAG-Replikationsvektor erzeugt, der das lacZ-Gen von E. coli, das für Beta-Galaktosidase (beta-gal) kodiert, und das Tn5-Neomycin-Gen, das eine Resistenz gegen G418 verleiht, trägt. Die Zelllinie 9L/lacZ zeichnet sich vor allem durch ihre Reportermarkierung aus, da sie das lacZ-Reportergen exprimiert. Dieses Reportergen ermöglicht die Visualisierung von beta-gal durch histochemische Färbung, was die Identifizierung einzelner Tumorzellen erleichtert und die Bildanalyse verbessert. Die in der biologischen Forschung weit verbreitete 9L/lacZ-Zelllinie findet Anwendung in der 3D-Zellkultur, bei der Entwicklung von Assays, im Hochdurchsatz-Screening und in neurowissenschaftlichen Studien. Sie dient als wertvolles Modell für die Untersuchung von Hirntumoren, da sie dem menschlichen Tumorwachstum sehr ähnlich ist und eine quantitative Analyse von mikroskopischen Tumoren ermöglicht. Diese adhärenten Zellen besitzen tumorigene Eigenschaften und können in Gehirnen von CD-Fischer-344-Ratten Tumore erzeugen, was sie zu einem hervorragenden Gliosarkom-Modell macht. Während die beta-gal-Expression stabil bleibt, kann eine erneute Klonierung für eine langfristige Aufrechterhaltung und konsistente experimentelle Ergebnisse erforderlich sein. |
|---|---|
| Organismus | Ratte |
| Gewebe | Gehirn |
| Krankheit | Malignes Gliom der Ratte |
| Synonyme | 9L/LacZ |
Merkmale
| Geschlecht | Männlich |
|---|---|
| Morphologie | Fibroblasten |
| Wachstumseigenschaften | Adhärent |
Identifikatoren / Biologische Schutzstufe / Zitation
| Zitat | 9L/lacZ (Cytion-Katalognummer 305208) |
|---|---|
| Biosicherheitsstufe | 1 |
Expression / Mutation
Handhabung
| Nährboden | DMEM, w: 4,5 g/L Glucose, w: 4 mM L-Glutamin, w: 1,5 g/L NaHCO3, w: 1,0 mM Natriumpyruvat (Cytion-Artikelnummer 820300a) |
|---|---|
| Mittlere Supplemente | Supplemente des Mediums mit 10% FBS |
| Passage-Lösung | Accutase |
| Subkultivierung | Entfernen Sie das alte Medium von den adhärenten Zellen und waschen Sie sie mit PBS, das kein Kalzium und Magnesium enthält. Für T25-Kolben 3-5 ml PBS und für T75-Kolben 5-10 ml verwenden. Anschließend werden die Zellen vollständig mit Accutase bedeckt, wobei 1-2 ml für T25-Kolben und 2,5 ml für T75-Kolben verwendet werden. Lassen Sie die Zellen 8-10 Minuten bei Raumtemperatur inkubieren, um sie abzulösen. Nach der Inkubation mischen Sie die Zellen vorsichtig mit 10 ml Medium, um sie zu resuspendieren, und zentrifugieren sie dann 3 Minuten lang bei 300xg. Den Überstand verwerfen, die Zellen in frischem Medium resuspendieren und in neue Kolben überführen, die bereits frisches Medium enthalten. |
| Splitverhältnis | 1:2 bis 1:5 |
| Medienwechsel | 2 bis 3 Mal pro Woche |
| Einfriermedium | CM-1 (Cytion Katalognummer 800100) oder CM-ACF (Cytion Katalognummer 806100) |
| Handhabung von kryokonservierten Kulturen |
|
Qualitätskontrolle / Genetisches Profil / HLA
| Sterilität | Eine Kontamination mit Mykoplasmen wird sowohl durch PCR-basierte Assays als auch durch lumineszenzbasierte Mykoplasmen-Nachweisverfahren ausgeschlossen. Um sicherzustellen, dass keine Kontamination mit Bakterien, Pilzen oder Hefen vorliegt, werden die Zellkulturen täglich visuell überprüft. |
|---|
