INS-1-Zellen












Produktnummer:
300471
Allgemeine Informationen
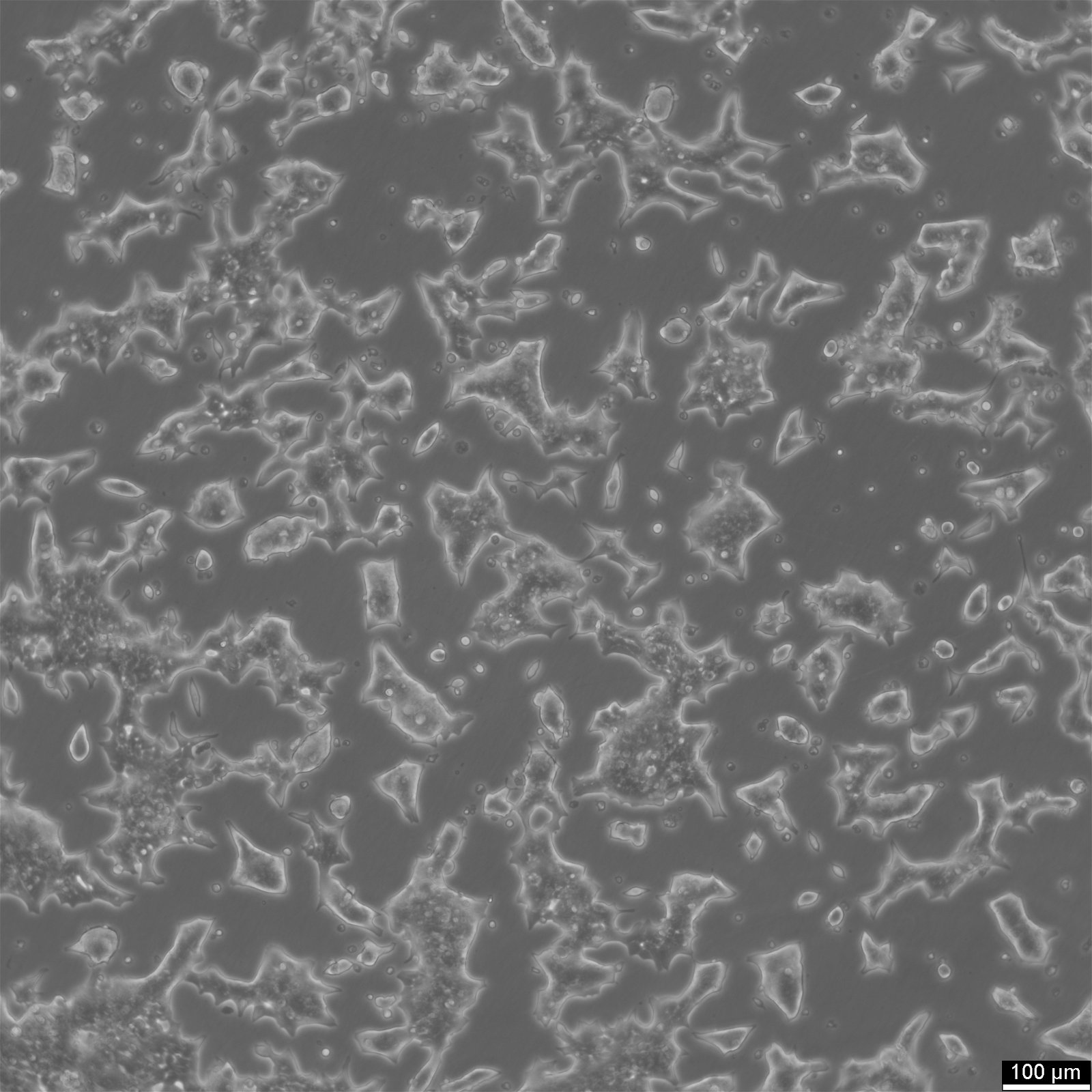
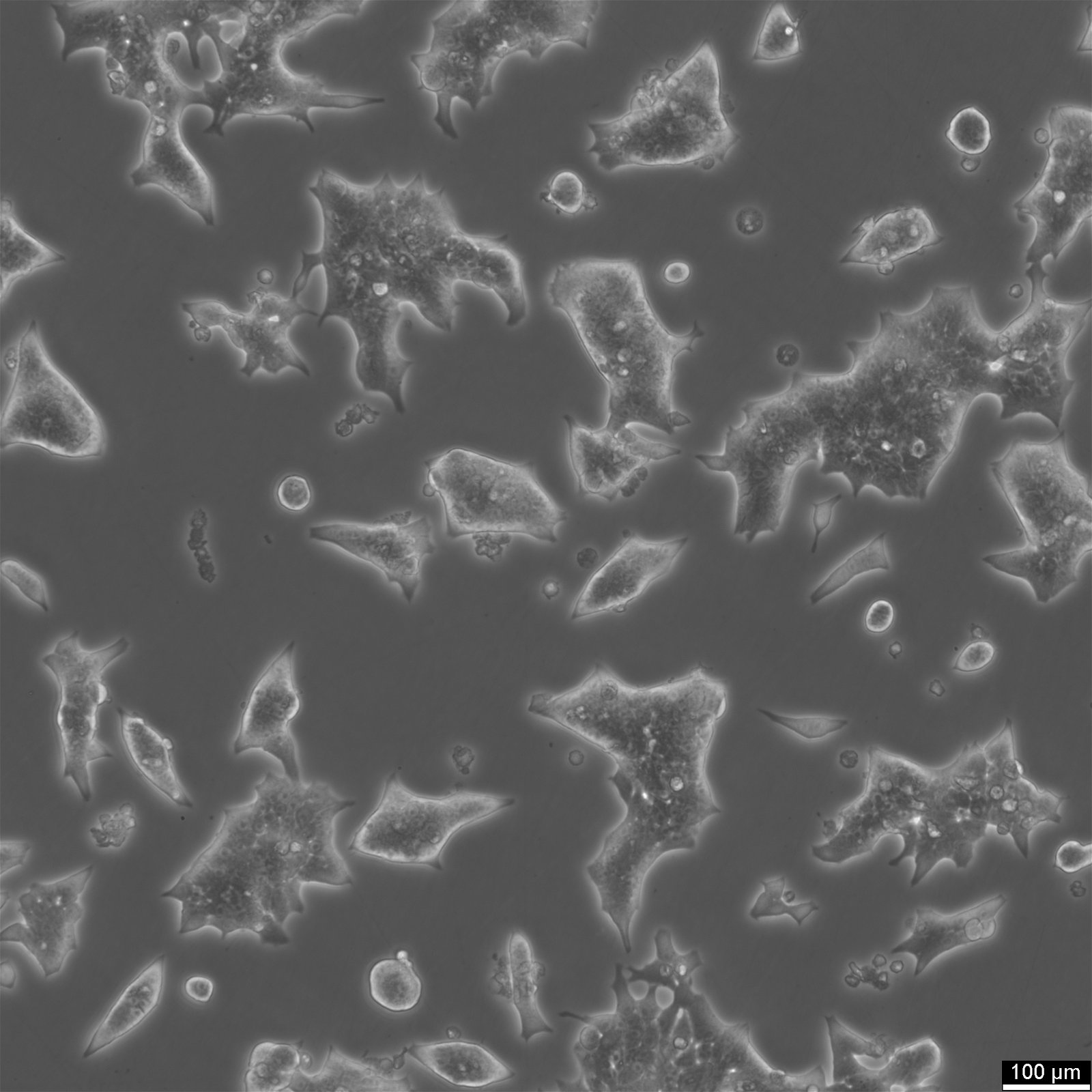
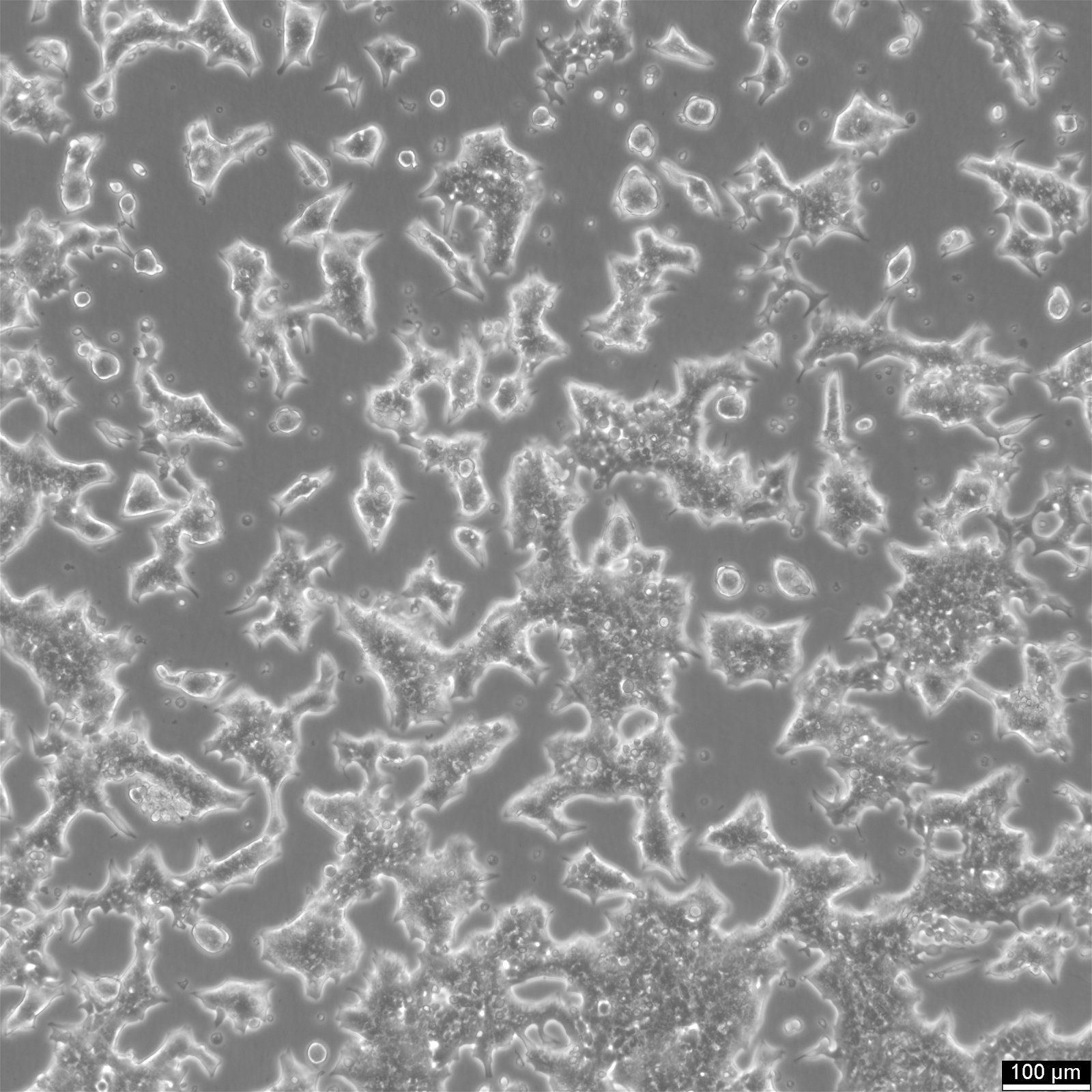
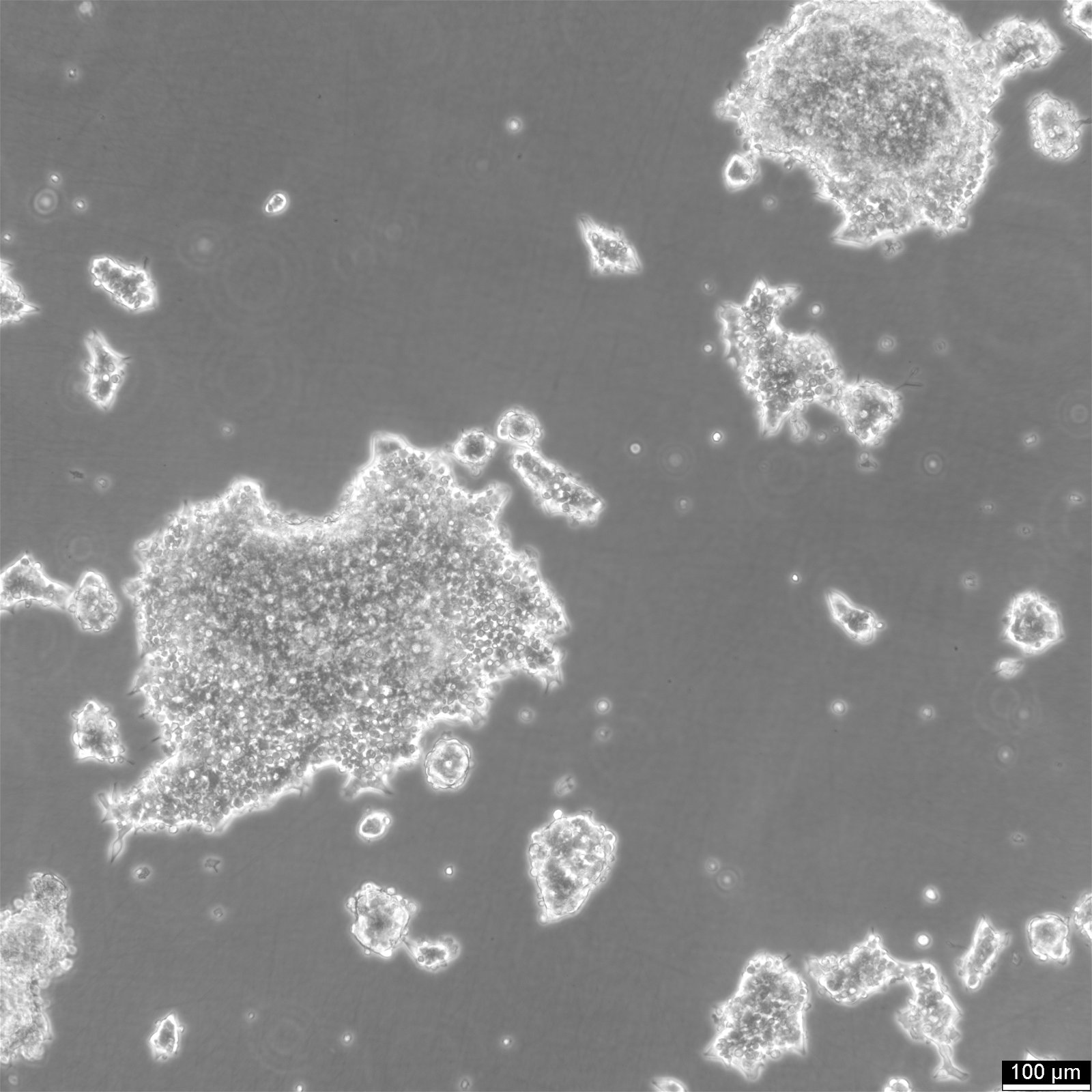
| Beschreibung | Die INS-1-Zelllinie stammt von einem durch Röntgenstrahlen erzeugten transplantierbaren Insulinom bei Ratten. Da INS-1-Zellen eine hohe Insulinkonzentration aufweisen und auf Veränderungen des Glukosespiegels reagieren, werden sie häufig zur Untersuchung der Funktion von Betazellen verwendet. Wachstum und Hormonexpression sind von dem Reduktionsmittel 2-Mercaptoethanol abhängig. INS-1-Zellen zeichnen sich durch ihre Heterogenität aus: Sie bestehen aus reifen insulinpositiven Zellen und unreifen bi-hormonalen Zellen, die Insulin- und Glucagonproteine exprimieren. Bi-hormonale INS-1-Zellen weisen eine geringere Nkx6.1-Expression auf und haben keine Alphazellmarker, was darauf hindeutet, dass sie noch nicht vollständig ausgereift sind. Darüber hinaus reduziert eine chronische Glukosestimulation die Insulin-Gen- und Protein-Expression in INS-1-Zellen. Infolgedessen sind die Spiegel von Insulin und von Proglucagon abgeleiteten Peptiden wie GLP-1, GLP-2 und Glucagon reduziert. |
|---|---|
| Organismus | Ratte |
| Gewebe | Bauchspeicheldrüse, Langerhans-Inseln |
| Krankheit | Insulinom der Ratte |
| Synonyme | INS1 |
Merkmale
| Alter | 666 Tage |
|---|---|
| Geschlecht | Männlich |
| Zelltyp | Betazelle |
| Wachstumseigenschaften | Adhärent/Suspension |
Identifikatoren / Biologische Schutzstufe / Zitation
| Zitat | INS-1 (Cytion Katalognummer 300471) |
|---|---|
| Biosicherheitsstufe | 1 |
Expression / Mutation
| Produkte | Insulin, Glutathion |
|---|
Handhabung
| Nährboden | RPMI 1640, w: 4,5 g/L Glucose, w: 2 mM L-Glutamin, w: 10 mM HEPES, w: 1 mM Natriumpyruvat, w: 1,5 g/L NaHCO3 (Cytion-Artikelnummer 820702a) |
|---|---|
| Mittlere Supplemente | Supplemente des Mediums mit 10% hitzeinaktiviertem FBS |
| Passage-Lösung | Accutase |
| Subkultivierung | Die Suspensionszellen in einem 15-ml-Röhrchen sammeln und die anhaftenden Zellen vorsichtig mit PBS ohne Kalzium und Magnesium waschen (3-5 ml für T25-Kolben und 5-10 ml für T75-Kolben verwenden). Accutase auftragen (1-2 ml für T25-Kolben, 2,5 ml für T75-Kolben), um sicherzustellen, dass die Zellschicht vollständig bedeckt ist. Die Zellen 10 Minuten lang bei Raumtemperatur inkubieren lassen. Nach der Inkubation sowohl die Suspension als auch die adhärenten Zellen mischen und zentrifugieren. Nach der Zentrifugation das Zellpellet vorsichtig resuspendieren und die Zellsuspension in neue Flaschen mit frischem Medium überführen. |
| Einfriermedium | CM-1 (Cytion Katalognummer 800100) oder CM-ACF (Cytion Katalognummer 806100) |
| Handhabung von kryokonservierten Kulturen | INS-1-Zellen werden in tiefgefrorenem Zustand auf Trockeneis versandt. Vergewissern Sie sich bei Erhalt, dass das Fläschchen gefroren ist. Lagern Sie das Kryovial sofort bei Temperaturen unter -150 Grad. Wenn Sie die Zellen sofort kultivieren wollen, tauen Sie das Fläschchen schnell auf, indem Sie es 40-60 Sekunden lang in einem 37 Grad warmen Wasserbad mit sauberem Wasser und einem antimikrobiellen Mittel schütteln. Entfernen Sie das Fläschchen, sobald sich ein kleiner Eisklumpen gebildet hat, und stellen Sie sicher, dass es kalt bleibt. Führen Sie alle weiteren Schritte unter aseptischen Bedingungen durch. Desinfizieren Sie das Kryovial unter einer sterilen Abzugshaube mit 70%igem Ethanol. Anschließend das Fläschchen vorsichtig öffnen und die Zellsuspension in ein 15-ml-Zentrifugenröhrchen überführen, das mit 8 ml Kulturmedium bei Raumtemperatur gefüllt ist. Die Zellen vorsichtig mischen. Zur Zellseparation 3 Minuten lang bei 300 x g zentrifugieren und den Überstand entsorgen. Das Auslassen der Zentrifugation ist fakultativ, allerdings sollten etwaige Reste des Gefriermediums nach 24 Stunden entfernt werden. Das Pellet vorsichtig in 10 ml frischem Kulturmedium resuspendieren und auf zwei T25-Kulturflaschen aufteilen. Für die weiteren Schritte das Subkulturprotokoll befolgen. |
Qualitätskontrolle / Genetisches Profil / HLA
| Sterilität | Eine Kontamination mit Mykoplasmen wird sowohl mit PCR-basierten Assays als auch mit lumineszenzbasierten Mykoplasmen-Nachweisverfahren rigoros ausgeschlossen. Um sicherzustellen, dass keine Kontamination mit Bakterien, Pilzen oder Hefen vorliegt, werden die Zellkulturen täglich visuell überprüft. |
|---|
